- Jan 19, 2026
L’eau intracellulaire : fluide, gel et énergie
- Morgane De Leye
De la mitochondrie au cytoplasme : ce que la science en dit actuellement
Introduction — Quand un mot interroge
Lors d’une conférence récente à laquelle j'ai participé sur la cellule, un terme a retenu mon attention : l’eau morphogénique.
Un mot beau, évocateur, presque poétique… mais aussi suffisamment flou pour éveiller mon esprit en quête de sens.
Lorsque l’on travaille avec le vivant les mots que l’on emploie ne sont jamais neutres. Ils façonnent notre compréhension, nos représentations, et parfois même nos pratiques.
Cet article n’a pas pour vocation de juger ni de discréditer. Il vise à clarifier.
À revenir à ce que la science observe, mesure et modélise actuellement concernant l’eau intracellulaire, le cytoplasme et la mitochondrie, et à comprendre ce que recouvre — ou non — le terme “eau morphogénique”.
1. La cellule n’est pas un sac d’eau
Pendant longtemps, la cellule a été décrite comme un simple compartiment rempli d’eau, dans lequel baignaient des protéines et des organites.
Cette vision est aujourd’hui dépassée.
L’eau intracellulaire n’est ni homogène, ni passive.
On distingue notamment :
L’eau libre, mobile,
L’eau interfaciale (ou hydration water), directement liée aux membranes, protéines et structures cellulaires.
Cette eau interfaciale possède :
Une dynamique différente de l’eau libre,
Des temps de relaxation modifiés,
Une interaction directe avec la conformation et l’activité des protéines.
Des techniques comme la résonance magnétique nucléaire (RMN) ou la diffusion neutronique ont permis de mesurer ces différences in vivo, montrant que l’eau intracellulaire est contrainte, organisée localement et fonctionnelle.
Autrement dit :
L’eau participe activement au fonctionnement cellulaire.
2. Le cytoplasme : un gel actif hydraté
Un matériau vivant, pas un liquide
Le cytoplasme n’est pas un simple liquide.
Il se comporte comme un matériau poroélastique : un réseau solide (cytosquelette, organites, macromolécules) imbibé d’une phase fluide (eau + solutés).
Dans ce modèle :
L’eau circule, mais elle est aussi retenue, canalisée, redistribuée selon les contraintes mécaniques.
Cette organisation permet :
La transmission des forces,
Le maintien de la forme cellulaire,
L'adaptation rapide aux contraintes de l’environnement.
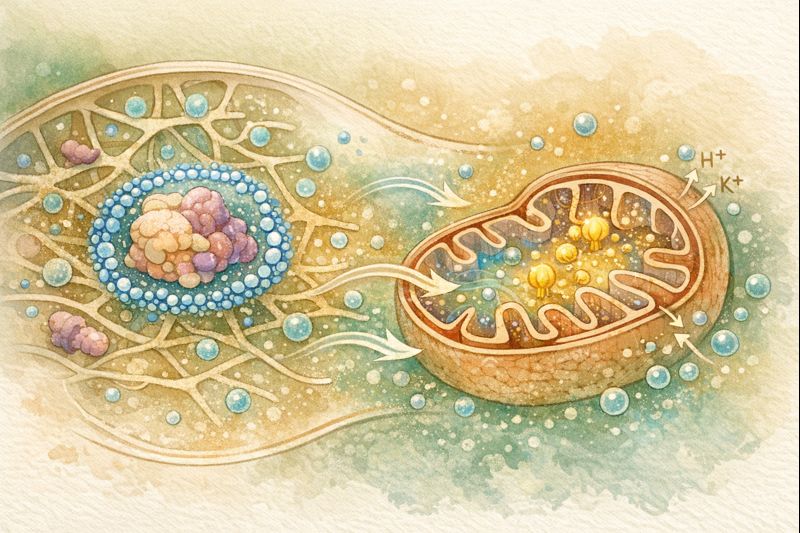
L’eau intracellulaire ne constitue pas un simple milieu passif. Elle interagit avec les protéines (eau interfaciale), le cytoplasme (gel actif poroélastique) et la mitochondrie (volume matriciel, énergie). C’est ce continuum eau–structure–énergie qui permet à la cellule de s’adapter, de maintenir sa forme et sa fonction.
3. Transitions gel ↔ sol : l’adaptabilité du vivant
Le cytoplasme peut passer :
d’un état plus gel, structuré, protecteur,
à un état plus sol, fluide, permissif.
Ces transitions dépendent notamment :
Du calcium,
Du pH,
De la disponibilité en ATP,
Du niveau de stress et de crowding moléculaire.
En situation de stress (hypoxie, acidose, inflammation), le cytoplasme peut devenir plus rigide, voire présenter des propriétés dites glassy.
À l’inverse, l’activité métabolique tend à fluidifier le cytoplasme.
La forme et la fonction cellulaire dépendent donc directement de l’état hydromécanique du cytoplasme.
4. La mitochondrie : eau, volume et énergie
Une matrice hautement hydratée et dynamique
La mitochondrie est souvent réduite à son rôle de “centrale énergétique”.
En réalité, c’est un espace hautement dynamique, où l’eau joue un rôle central.
La matrice mitochondriale :
est fortement hydratée,
voit son volume varier en fonction des flux ioniques (H⁺, K⁺, Ca²⁺),
est sensible aux phénomènes osmotiques.
Certaines études suggèrent que :
la membrane mitochondriale interne est hautement perméable à l’eau,
et que l’eau métabolique produite lors de la respiration pourrait contribuer à la régulation du volume matriciel.
5. Quand l’eau conditionne l’énergie
L’état d’hydratation de la matrice influence :
la viscosité,
le crowding mitochondrial,
la diffusion des substrats et enzymes,
l’efficacité de la chaîne respiratoire.
Sous stress oxydatif ou métabolique, la matrice devient plus dense, plus visqueuse, ce qui altère la production énergétique.
La mitochondrie n’est donc pas qu’un producteur d’ATP :
elle est un nœud de régulation eau–énergie–structure.
6. Alors, qu’est-ce que “l'eau morphogénique” ?
Un terme non scientifique, mais une intuition réelle
Le terme “eau morphogénique” n’existe pas en tant que tel dans la littérature scientifique.
Il s’agit d’un mot-pont, souvent utilisé en conférence pour désigner une réalité complexe :
une eau qui participe à l’organisation, à la forme et à la fonction du vivant.
Cette intuition n’est pas fausse.
Mais le mot peut devenir trompeur s’il laisse entendre l’existence d’une eau dotée, à elle seule, d’une intention ou d’une information autonome.
Pourquoi cette information est essentielle pour les thérapeutes
Pour les praticiens du soin et de l’accompagnement, cette clarté est fondamentale.
Elle permet :
une compréhension fine du stress cellulaire,
une lecture plus juste de la fatigue mitochondriale,
une approche nuancée de l’inflammation chronique,
une intégration cohérente des pratiques corporelles, respiratoires, nutritionnelles et somatiques.
Travailler avec le vivant demande à la fois :
ouverture,
et discernement.
C’est dans cet équilibre que naît une pratique juste, incarnée et respectueuse du réel biologique.
Conclusion — Honorer la complexité du vivant
L’eau dans la cellule est un état complexe extraordinaire.
Elle est :
structurée,
contrainte,
dynamique,
intimement liée à la forme, à l’énergie et à l’adaptation du vivant.
Comprendre cela, c’est honorer la cellule comme un système d’une intelligence remarquable, que la science continue — humblement — d’explorer.
📚 Bibliographie
Eau intracellulaire & eau interfaciale
Jasnin, M., Stadler, A. M., Tehei, M., & Zaccai, G. (2010).
Specific cellular water dynamics observed in vivo by neutron scattering and NMR.
Physical Chemistry Chemical Physics, 12(36), 10154–10160.
https://doi.org/10.1039/C0CP01048K
Jasnin, M., Moulin, M., Haertlein, M., Zaccai, G., & Tehei, M. (2008).
Down to atomic-scale intracellular water dynamics.
EMBO Reports, 9(6), 543–547.
https://doi.org/10.1038/embor.2008.64
Laage, D., Elsaesser, T., & Hynes, J. T. (2017).
Water dynamics in the hydration shells of biomolecules.
Chemical Reviews, 117(16), 10694–10725.
https://doi.org/10.1021/acs.chemrev.6b00765
Qvist, J., Persson, E., Mattea, C., & Halle, B. (2009).
Time scales of water dynamics at biological interfaces: peptides, proteins and cells.
Faraday Discussions, 141, 131–144.
https://doi.org/10.1039/B806194G
Cytoplasme : gel actif, poroélasticité, transitions mécaniques
Moeendarbary, E., Valon, L., Fritzsche, M., Harris, A. R., Moulding, D. A., Thrasher, A. J., … Charras, G. T. (2013).
The cytoplasm of living cells behaves as a poroelastic material.
Nature Materials, 12(3), 253–261.
https://doi.org/10.1038/nmat3517
Parry, B. R., Surovtsev, I. V., Cabeen, M. T., O’Hern, C. S., Dufresne, E. R., & Jacobs-Wagner, C. (2014).
The bacterial cytoplasm has glass-like properties and is fluidized by metabolic activity.
Cell, 156(1–2), 183–194.
https://doi.org/10.1016/j.cell.2013.11.028
Munder, M. C., Midtvedt, D., Franzmann, T., Nüske, E., Otto, O., Herbig, M., … Alberti, S. (2016).
A pH-driven transition of the cytoplasm from a fluid- to a solid-like state promotes entry into dormancy.
eLife, 5, e09347.
https://doi.org/10.7554/eLife.09347
Umeda, K., Shimamoto, Y., & Kimura, A. (2023).
Activity-dependent glassy cell mechanics: Nonthermal fluctuations under metabolic activity.
Biophysical Journal, 122(3), 521–533.
https://doi.org/10.1016/j.bpj.2022.12.028
Yin, H. L., & Stossel, T. P. (1979).
Control of cytoplasmic actin gel–sol transformation by gelsolin, a calcium-dependent regulatory protein.
Nature, 281(5732), 583–586.
https://doi.org/10.1038/281583a0
Mitochondrie : eau, volume matriciel, crowding, bioénergétique
Kaasik, A., & Safiulina, D. (2007).
Regulation of mitochondrial matrix volume.
American Journal of Physiology – Cell Physiology, 292(5), C157–C163.
https://doi.org/10.1152/ajpcell.00272.2006
Casteilla, L., Rigoulet, M., & Pénicaud, L. (2011).
Control of mitochondrial volume by mitochondrial metabolic water.
Mitochondrion, 11(6), 862–866.
https://doi.org/10.1016/j.mito.2011.06.008
Dieteren, C. E. J., Gielen, S. C. A. M., Nijtmans, L. G. J., Smeitink, J. A. M., & Swarts, H. G. P. (2011).
Solute diffusion is hindered in the mitochondrial matrix.
Proceedings of the National Academy of Sciences, 108(21), 8657–8662.
https://doi.org/10.1073/pnas.1017581108
Bulthuis, E. P., Adjobo-Hermans, M. J. W., Willems, P. H. G. M., & Koopman, W. J. H. (2023).
Stress-dependent macromolecular crowding in the mitochondrial matrix.
The EMBO Journal, 42(3), e110853.
https://doi.org/10.15252/embj.202110853
Austin, S., et al. (2021).
Mitochondrial osmoregulation in evolution, cation transport and metabolism.
Biochimica et Biophysica Acta (BBA) – Bioenergetics, 1862(9), 148404.
https://doi.org/10.1016/j.bbabio.2021.148404
Eau structurée & débats scientifiques (cadre critique)
Elton, D. C., & Spencer, P. D. (2020).
Critical review of the evidence for exclusion zones around hydrophilic surfaces.
Journal of Physical Chemistry B, 124(10), 2129–2143.
https://doi.org/10.1021/acs.jpcb.9b10743
- 450 € ou 3 paiements mensuels de 150 €
Programme complet d’accompagnement de la gestion traumatique et résilience
- Fermé
- Paquet
- 4 Produits
- 80 €
Mentorat et coaching personnalisé – Accompagnement du thérapeute
- Séance de coaching
Inscris toi à la Newsletter
Si tu veux recevoir les dernières info sur les cours ou sur les prochains posts